Lantus para el tratamiento de la diabetes
Nombre de la marca: Lantus
Nombre genérico: insulina glargina
Forma de dosificación: Inyección (Lantus NO debe diluirse ni mezclarse con ninguna otra insulina o solución)
Contenido:
Descripción
Farmacología Clínica
Indicaciones y uso
Contraindicaciones
Advertencias
Precauciones
Reacciones adversas
Dosificación y administración
Cómo se suministra
Lantus, insulina glargina (origen de ADNr), información del paciente (en inglés simple)
Descripción
Lantus® (inyección de insulina glargina [origen de ADNr]) es una solución estéril de insulina glargina para usar como inyección. La insulina glargina es un análogo de insulina humana recombinante que es un agente reductor de la glucosa en sangre parenteral de acción prolongada (hasta 24 horas de acción). (Ver FARMACOLOGÍA CLÍNICA). Lantus se produce mediante tecnología de ADN recombinante que utiliza una cepa de laboratorio no patógena de Escherichia coli (K12) como organismo de producción. La insulina glargina difiere de la insulina humana en que el aminoácido asparagina en la posición A21 se reemplaza por glicina y se añaden dos argininas al extremo C de la cadena B. Químicamente, es 21A-Gly-30Ba-L-Arg-30Bb-L-Arg-insulina humana y tiene la fórmula empírica C267H404N72O78S6 y un peso molecular de 6063. Tiene la siguiente fórmula estructural:

Lantus consiste en insulina glargina disuelta en un líquido acuoso transparente. Cada mililitro de Lantus (inyección de insulina glargina) contiene 100 UI (3,6378 mg) de insulina glargina.
Los ingredientes inactivos para el vial de 10 ml son 30 mcg de zinc, 2,7 mg de m-cresol, 20 mg de glicerol al 85%, 20 mcg de polisorbato 20 y agua para inyección.
Los ingredientes inactivos para el cartucho de 3 ml son 30 mcg de zinc, 2,7 mg de m-cresol, 20 mg de glicerol al 85% y agua para inyección.
El pH se ajusta mediante la adición de soluciones acuosas de ácido clorhídrico e hidróxido de sodio. Lantus tiene un pH de aproximadamente 4.
parte superior
Farmacología Clínica
Mecanismo de acción
La actividad principal de la insulina, incluida la insulina glargina, es la regulación del metabolismo de la glucosa. La insulina y sus análogos reducen los niveles de glucosa en la sangre al estimular la absorción periférica de glucosa, especialmente por el músculo esquelético y la grasa, e inhibiendo la producción de glucosa hepática. La insulina inhibe la lipólisis en el adipocito, inhibe la proteólisis y mejora la síntesis de proteínas.
Farmacodinámica
La insulina glargina es un análogo de insulina humana que se ha diseñado para tener una baja solubilidad acuosa a pH neutro. A pH 4, como en la solución de inyección de Lantus, es completamente soluble. Después de la inyección en el tejido subcutáneo, la solución ácida se neutraliza, lo que lleva a la formación de microprecipitados a partir de los cuales se liberan lentamente cantidades de insulina glargina, lo que resulta en un perfil de concentración / tiempo relativamente constante durante 24 horas sin pronunciamiento pico. Este perfil permite la dosificación una vez al día como insulina basal del paciente.
En estudios clínicos, el efecto reductor de glucosa en una base molar (es decir, cuando se administra a las mismas dosis) de insulina glargina intravenosa es aproximadamente el mismo que la insulina humana. En estudios de pinzamiento euglucémico en sujetos sanos o en pacientes con diabetes tipo 1, el inicio de acción de la insulina glargina subcutánea fue más lento que la insulina humana NPH. El perfil del efecto de la insulina glargina fue relativamente constante sin un pico pronunciado y la duración de su efecto se prolongó en comparación con la insulina humana NPH. La Figura 1 muestra los resultados de un estudio en pacientes con diabetes tipo 1 realizado durante un máximo de 24 horas después de la inyección. La mediana del tiempo entre la inyección y el final del efecto farmacológico fue de 14.5 horas (rango: 9.5 a 19.3 horas) para NPH insulina humana y 24 horas (rango: 10.8 a> 24.0 horas) (24 horas fue el final del período de observación) para insulina glargina
Figura 1. Perfil de actividad en pacientes con diabetes tipo 1
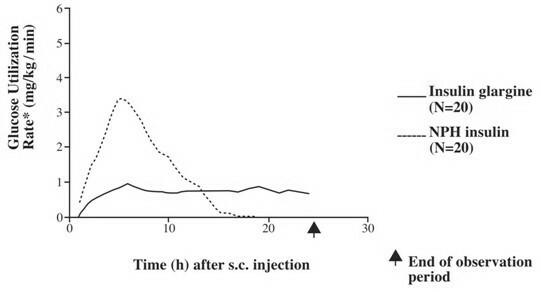
* Determinado como la cantidad de glucosa infundida para mantener niveles constantes de glucosa en plasma (valores medios por hora); indicativo de actividad de insulina.
⠀ Variabilidad entre pacientes (CV, coeficiente de variación); insulina glargina, 84% y NPH, 78%.
La mayor duración de acción (hasta 24 horas) de Lantus está directamente relacionada con su velocidad de absorción más lenta y es compatible con la administración subcutánea una vez al día. El curso temporal de acción de las insulinas, incluida Lantus, puede variar entre individuos y / o dentro del mismo individuo.
Farmacocinética
Absorción y biodisponibilidad
Después de la inyección subcutánea de insulina glargina en sujetos sanos y en pacientes con diabetes, las concentraciones séricas de insulina indicaron un absorción más lenta y prolongada y un perfil de concentración / tiempo relativamente constante durante 24 horas sin pico pronunciado en comparación con NPH humano insulina. Las concentraciones séricas de insulina fueron consistentes con el perfil de tiempo de la actividad farmacodinámica de la insulina glargina.
Después de la inyección subcutánea de 0.3 UI / kg de insulina glargina en pacientes con diabetes tipo 1, se ha demostrado un perfil de concentración / tiempo relativamente constante. La duración de la acción después de la administración subcutánea abdominal, deltoidea o del muslo fue similar.
Metabolismo
Un estudio del metabolismo en humanos indica que la insulina glargina se metaboliza en parte en el extremo carboxilo de la cadena B en la vía subcutánea. depósito para formar dos metabolitos activos con actividad in vitro similar a la de la insulina, M1 (21A-Gly-insulin) y M2 (21A-Gly-des-30B-Thr-insulina). El fármaco inalterado y estos productos de degradación también están presentes en la circulación.
Poblaciones Especiales
Edad, raza y género
La información sobre el efecto de la edad, la raza y el género en la farmacocinética de Lantus no está disponible. Sin embargo, en ensayos clínicos controlados en adultos (n = 3890) y en un ensayo clínico controlado en pacientes pediátricos (n = 349), subgrupo Los análisis basados en la edad, la raza y el género no mostraron diferencias en seguridad y eficacia entre la insulina glargina y la NPH humana. insulina.
De fumar
No se ha estudiado el efecto del tabaquismo sobre la farmacocinética / farmacodinámica de Lantus.
El embarazo
No se ha estudiado el efecto del embarazo sobre la farmacocinética y farmacodinámica de Lantus (ver PRECAUCIONES, El embarazo).
Obesidad
En ensayos clínicos controlados, que incluyeron pacientes con índice de masa corporal (IMC) de hasta 49,6 kg / m2, Los análisis de subgrupos basados en el IMC no mostraron diferencias en la seguridad y la eficacia entre la insulina glargina y la NPH humana insulina.
Insuficiencia renal
No se ha estudiado el efecto de la insuficiencia renal sobre la farmacocinética de Lantus. Sin embargo, algunos estudios con insulina humana han demostrado un aumento de los niveles circulantes de insulina en pacientes con insuficiencia renal. La monitorización cuidadosa de la glucosa y los ajustes de dosis de insulina, incluida Lantus, pueden ser necesarios en pacientes con disfunción renal (ver PRECAUCIONES, Insuficiencia renal).
Deterioro hepático
No se ha estudiado el efecto de la insuficiencia hepática en la farmacocinética de Lantus. Sin embargo, algunos estudios con insulina humana han demostrado un aumento de los niveles circulantes de insulina en pacientes con insuficiencia hepática. La monitorización cuidadosa de la glucosa y los ajustes de dosis de insulina, incluida Lantus, pueden ser necesarios en pacientes con disfunción hepática (ver PRECAUCIONES, Deterioro hepático).
Estudios clínicos
La seguridad y eficacia de la insulina glargina administrada una vez al día a la hora de acostarse se comparó con la de la insulina humana NPH una vez al día y dos veces al día en una etiqueta abierta, aleatorizada, control activo, estudios paralelos de 2327 pacientes adultos y 349 pacientes pediátricos con diabetes mellitus tipo 1 y 1563 pacientes adultos con diabetes mellitus tipo 2 (ver Tablas 1-3). En general, la reducción de la hemoglobina glucosilada (HbA1c) con Lantus fue similar a la de la insulina humana NPH. Las tasas generales de hipoglucemia no difirieron entre los pacientes con diabetes tratados con Lantus en comparación con la insulina humana NPH.
Diabetes tipo 1 para adultos (ver Tabla 1).
En dos grandes estudios clínicos aleatorizados y controlados (Estudios A y B), pacientes con diabetes tipo 1 (Estudio A; n = 585, estudio B; n = 534) fueron asignados al azar al tratamiento de bolo basal con Lantus una vez al día antes de acostarse o a insulina humana NPH una o dos veces al día y tratados durante 28 semanas. Se administró insulina humana regular antes de cada comida. Lantus se administró a la hora de acostarse. La insulina humana NPH se administró una vez al día al acostarse o por la mañana y al acostarse cuando se usó dos veces al día. En un estudio clínico grande, aleatorizado y controlado (Estudio C), pacientes con diabetes tipo 1 (n = 619) fueron tratados durante 16 semanas con un régimen de insulina en bolo basal donde se utilizó insulina lispro antes de cada comida. Lantus se administró una vez al día antes de acostarse y la insulina humana NPH se administró una o dos veces al día. En estos estudios, Lantus y la insulina humana NPH tuvieron un efecto similar sobre la glucohemoglobina con una tasa general de hipoglucemia similar.
Tabla 1: Diabetes mellitus tipo 1-Adulto
| Estudio A | Estudio B | Estudio c | ||||
|---|---|---|---|---|---|---|
| Duración del tratamiento | 28 semanas | 28 semanas | 16 semanas | |||
| Tratamiento en combinación con | Insulina regular | Insulina regular | Insulina lispro | |||
| Lantus | NPH | Lantus | NPH | Lantus | NPH | |
| Número de sujetos tratados | 292 | 293 | 264 | 270 | 310 | 309 |
| HbA1c | ||||||
| Endstudy mean | 8.13 | 8.07 | 7.55 | 7.49 | 7.53 | 7.60 |
| Adj. cambio medio desde el inicio | +0.21 | +0.10 | -0.16 | -0.21 | -0.07 | -0.08 |
| Lantus - NPH | +0.11 | +0.05 | +0.01 | |||
| IC del 95% para diferencia de tratamiento | (-0.03; +0.24) | (-0.08; +0.19) | (-0.11; +0.13) | |||
| Dosis basal de insulina | ||||||
| Endstudy mean | 19.2 | 22.8 | 24.8 | 31.3 | 23.9 | 29.2 |
| Cambio medio desde el inicio | -1.7 | -0.3 | -4.1 | +1.8 | -4.5 | +0.9 |
| Dosis total de insulina | ||||||
| Endstudy mean | 46.7 | 51.7 | 50.3 | 54.8 | 47.4 | 50.7 |
| Cambio medio desde el inicio | -1.1 | -0.1 | +0.3 | +3.7 | -2.9 | +0.3 |
| Glucemia en ayunas (mg / dL) | ||||||
| Endstudy mean | 146.3 | 150.8 | 147.8 | 154.4 | 144.4 | 161.3 |
| Adj. cambio medio desde el inicio | -21.1 | -16.0 | -20.2 | -16.9 | -29.3 | -11.9 |
Diabetes tipo 1 pediátrica (ver Tabla 2).
En un estudio clínico aleatorizado y controlado (Estudio D), pacientes pediátricos (rango de edad de 6 a 15 años) con diabetes tipo 1 (n = 349) fueron tratados durante 28 semanas con un régimen de insulina en bolo basal donde se usó insulina humana regular antes de cada comida. Lantus se administró una vez al día antes de acostarse y la insulina humana NPH se administró una o dos veces al día. Se observaron efectos similares sobre la glucohemoglobina y la incidencia de hipoglucemia en ambos grupos de tratamiento.
Tabla 2: Diabetes mellitus tipo 1 pediátrica
| Estudio d | ||
|---|---|---|
| Duración del tratamiento | 28 semanas | |
| Tratamiento en combinación con | Insulina regular | |
| Lantus | NPH | |
| Número de sujetos tratados | 174 | 175 |
| HbA1c | ||
| Endstudy mean | 8.91 | 9.18 |
| Adj. cambio medio desde el inicio | +0.28 | +0.27 |
| Lantus - NPH | +0.01 | |
| IC del 95% para diferencia de tratamiento | (-0.24; +0.26) | |
| Dosis basal de insulina | ||
| Endstudy mean | 18.2 | 21.1 |
| Cambio medio desde el inicio | -1.3 | +2.4 |
| Dosis total de insulina | ||
| Endstudy mean | 45.0 | 46.0 |
| Cambio medio desde el inicio | +1.9 | +3.4 |
| Glucemia en ayunas (mg / dL) | ||
| Endstudy mean | 171.9 | 182.7 |
| Adj. cambio medio desde el inicio | -23.2 | -12.2 |
Diabetes tipo 2 en adultos (ver Tabla 3).
En un gran estudio clínico aleatorizado y controlado (Estudio E) (n = 570), se evaluó a Lantus durante 52 semanas como parte de un régimen de terapia combinada con insulina y agentes antidiabéticos orales (una sulfonilurea, metformina, acarbosa o combinaciones de estos drogas). Lantus administrado una vez al día a la hora de acostarse fue tan eficaz como la insulina humana NPH administrada una vez al día a la hora de acostarse para reducir la glucohemoglobina y la glucosa en ayunas. Hubo una baja tasa de hipoglucemia que fue similar en pacientes tratados con insulina humana Lantus y NPH. En un estudio clínico grande, aleatorizado y controlado (Estudio F), en pacientes con diabetes tipo 2 que no usan agentes antidiabéticos orales (n = 518), se evaluó un régimen de bolo basal de Lantus una vez al día a la hora de acostarse o insulina humana NPH administrada una o dos veces al día 28 semanas Se usó insulina humana regular antes de las comidas según fuera necesario. Lantus tuvo una efectividad similar a la insulina humana NPH una o dos veces al día para reducir la glucohemoglobina y la glucosa en ayunas con una incidencia similar de hipoglucemia.
Tabla 3: Diabetes mellitus tipo 2-Adulto
| Estudio E | Estudio F | |||
|---|---|---|---|---|
| Duración del tratamiento | 52 semanas | 28 semanas | ||
| Tratamiento en combinación con | Agentes orales | Insulina regular | ||
| Lantus | NPH | Lantus | NPH | |
| Número de sujetos tratados | 289 | 281 | 259 | 259 |
| HbA1c | ||||
| Endstudy mean | 8.51 | 8.47 | 8.14 | 7.96 |
| Adj. cambio medio desde el inicio | -0.46 | -0.38 | -0.41 | -0.59 |
| Lantus - NPH | -0.08 | +0.17 | ||
| IC del 95% para diferencia de tratamiento | (-0.28; +0.12) | (-0.00; +0.35) | ||
| Dosis basal de insulina | ||||
| Endstudy mean | 25.9 | 23.6 | 42.9 | 52.5 |
| Cambio medio desde el inicio | +11.5 | +9.0 | -1.2 | +7.0 |
| Dosis total de insulina | ||||
| Endstudy mean | 25.9 | 23.6 | 74.3 | 80.0 |
| Cambio medio desde el inicio | +11.5 | +9.0 | +10.0 | +13.1 |
| Glucemia en ayunas (mg / dL) | ||||
| Endstudy mean | 126.9 | 129.4 | 141.5 | 144.5 |
| Adj. cambio medio desde el inicio | -49.0 | -46.3 | -23.8 | -21.6 |
Dosificación diaria flexible de Lantus
La seguridad y eficacia de Lantus administrada antes del desayuno, antes de la cena o antes de acostarse fueron evaluado en un estudio clínico grande, aleatorizado y controlado, en pacientes con diabetes tipo 1 (estudio G, n = 378). Los pacientes también fueron tratados con insulina lispro a la hora de las comidas. Lantus administrado en diferentes momentos del día produjo reducciones similares en la hemoglobina glucosilada en comparación con la administración a la hora de acostarse (ver Tabla 4). En estos pacientes, los datos están disponibles a partir de la monitorización de glucosa en el hogar de 8 puntos. El nivel medio máximo de glucosa en sangre se observó justo antes de la inyección de Lantus, independientemente del momento de la administración, es decir, antes del desayuno, antes de la cena o antes de acostarse.
En este estudio, el 5% de los pacientes en el grupo de desayuno Lantus interrumpió el tratamiento debido a la falta de eficacia. Ningún paciente en los otros dos brazos interrumpió por este motivo. El monitoreo rutinario durante este ensayo reveló los siguientes cambios medios en la presión arterial sistólica: grupo antes del desayuno, 1.9 mm Hg; grupo previo a la cena, 0.7 mm Hg; grupo antes de acostarse, -2.0 mm Hg.
La seguridad y eficacia de Lantus administrado antes del desayuno o al acostarse también se evaluaron en un estudio grande, aleatorizado, estudio clínico controlado activo (Estudio H, n = 697) en pacientes con diabetes tipo 2 que ya no se controla adecuadamente con el agente oral terapia. Todos los pacientes en este estudio también recibieron AMARYL® (glimepirida) 3 mg al día. Lantus administrada antes del desayuno fue al menos tan efectiva para reducir la hemoglobina glucosilada A1c (HbA1c) como Lantus administrada antes de acostarse o la insulina humana NPH administrada antes de acostarse (ver Tabla 4).
Tabla 4: Dosificación diaria flexible de Lantus en diabetes mellitus tipo 1 (estudio G) y tipo 2 (estudio H)
| Estudio g | Estudio h | |||||
|---|---|---|---|---|---|---|
| Duración del tratamiento | 24 semanas | 24 semanas | ||||
| Tratamiento en combinación con: | Insulina lispro | AMARYL® (glimepirida) | ||||
| Lantus Desayuno |
Lantus Cena |
Lantus Hora de acostarse |
Lantus Desayuno |
Lantus Hora de acostarse |
NPH Hora de acostarse |
|
| ||||||
| Número de sujetos tratados* | 112 | 124 | 128 | 234 | 226 | 227 |
| HbA1c | ||||||
| Media basal | 7.56 | 7.53 | 7.61 | 9.13 | 9.07 | 9.09 |
| Endstudy mean | 7.39 | 7.42 | 7.57 | 7.87 | 8.12 | 8.27 |
| Cambio medio desde el inicio | -0.17 | -0.11 | -0.04 | -1.26 | -0.95 | -0.83 |
| Dosis basal de insulina (UI) | ||||||
| Endstudy mean | 27.3 | 24.6 | 22.8 | 40.4 | 38.5 | 36.8 |
| Cambio medio desde el inicio | 5.0 | 1.8 | 1.5 | |||
| Dosis total de insulina (UI) | NAâ € | N / A | N / A | |||
| Endstudy mean | 53.3 | 54.7 | 51.5 | |||
| Cambio medio desde el inicio | 1.6 | 3.0 | 2.3 |
parte superior
Indicaciones y uso
Lantus está indicado para administración subcutánea una vez al día para el tratamiento de pacientes adultos y pediátricos con tipo 1 diabetes mellitus o pacientes adultos con diabetes mellitus tipo 2 que requieren insulina basal (de acción prolongada) para el control de hiperglucemia
parte superior
Contraindicaciones
Lantus está contraindicado en pacientes hipersensibles a la insulina glargina o los excipientes.
parte superior
Advertencias
La hipoglucemia es el efecto adverso más común de la insulina, incluida Lantus. Como con todas las insulinas, el momento de la hipoglucemia puede diferir entre varias formulaciones de insulina. La monitorización de glucosa se recomienda para todos los pacientes con diabetes.
Cualquier cambio de insulina debe hacerse con precaución y solo bajo supervisión médica. Cambios en la intensidad de la insulina, el momento de la dosificación, el fabricante, el tipo (por ejemplo, regular, NPH o análogos de insulina), especie (animal, humano), o el método de fabricación (ADN recombinante versus insulina de origen animal) puede resultar en la necesidad de un cambio en Dosis. Es posible que sea necesario ajustar el tratamiento concomitante con antidiabéticos orales.
parte superior
Precauciones
General
Lantus no está destinado a la administración intravenosa. La duración prolongada de la actividad de la insulina glargina depende de la inyección en el tejido subcutáneo. La administración intravenosa de la dosis subcutánea habitual puede provocar hipoglucemia grave.
Lantus NO debe diluirse ni mezclarse con ninguna otra insulina o solución. Si Lantus se diluye o se mezcla, la solución puede volverse turbia y el perfil farmacocinético / farmacodinámico. (p. ej., inicio de acción, tiempo hasta el efecto máximo) de Lantus y / o la insulina mixta puede alterarse de forma impredecible conducta. Cuando Lantus y la insulina humana regular se mezclaron inmediatamente antes de la inyección en perros, se observó un inicio tardío de la acción y el tiempo hasta el efecto máximo para la insulina humana regular. La biodisponibilidad total de la mezcla también disminuyó ligeramente en comparación con las inyecciones separadas de Lantus y la insulina humana regular. Se desconoce la relevancia de estas observaciones en perros para humanos.
Al igual que con todas las preparaciones de insulina, el curso temporal de la acción de Lantus puede variar en diferentes individuos o en diferentes veces en el mismo individuo y la tasa de absorción depende del suministro de sangre, la temperatura y el físico actividad.
La insulina puede causar retención de sodio y edema, particularmente si el control metabólico previamente pobre mejora con la terapia intensiva de insulina.
Hipoglucemia
Como con todas las preparaciones de insulina, las reacciones hipoglucémicas pueden estar asociadas con la administración de Lantus. La hipoglucemia es el efecto adverso más común de las insulinas. Los síntomas de advertencia temprana de hipoglucemia pueden ser diferentes o menos pronunciados bajo ciertas condiciones, como por ejemplo duración de la diabetes, enfermedad del nervio diabético, uso de medicamentos como betabloqueantes o control intensificado de la diabetes (ver PRECAUCIONES, Interacciones con la drogas). Tales situaciones pueden resultar en hipoglucemia severa (y, posiblemente, pérdida de conciencia) antes de que los pacientes estén conscientes de la hipoglucemia.
El tiempo de aparición de hipoglucemia depende del perfil de acción de las insulinas utilizadas y, por lo tanto, puede cambiar cuando se cambia el régimen de tratamiento o el momento de la dosificación. Los pacientes que cambian de insulina NPH dos veces al día a Lantus una vez al día deben tener su inicial La dosis de Lantus se redujo en un 20% de la dosis diaria total de NPH previa para reducir el riesgo de hipoglucemia (ver DOSIFICACIÓN Y ADMINISTRACIÓN, Cambio a Lantus).
El efecto prolongado de Lantus subcutáneo puede retrasar la recuperación de la hipoglucemia.
En un estudio clínico, los síntomas de hipoglucemia o respuestas hormonales contrarreguladoras fueron similares después de insulina glargina intravenosa e insulina humana regular tanto en sujetos sanos como en pacientes con tipo 1 diabetes.
Insuficiencia renal
Aunque no se han realizado estudios en pacientes con diabetes e insuficiencia renal, los requisitos de Lantus puede disminuir debido al metabolismo reducido de la insulina, similar a las observaciones encontradas con otras insulinas (ver FARMACOLOGÍA CLÍNICA, Poblaciones especiales).
Deterioro hepático
Aunque no se han realizado estudios en pacientes con diabetes e insuficiencia hepática, los requisitos de Lantus pueden disminuir. debido a la capacidad reducida de gluconeogénesis y al metabolismo reducido de la insulina, similar a las observaciones encontradas con otras insulinas (ver FARMACOLOGÍA CLÍNICA, Poblaciones especiales).
Sitio de inyección y reacciones alérgicas
Al igual que con cualquier terapia con insulina, la lipodistrofia puede ocurrir en el sitio de inyección y retrasar la absorción de insulina. Otras reacciones en el sitio de inyección con la terapia con insulina incluyen enrojecimiento, dolor, picazón, urticaria, hinchazón e inflamación. La rotación continua del sitio de inyección dentro de un área determinada puede ayudar a reducir o prevenir estas reacciones. La mayoría de las reacciones menores a las insulinas generalmente se resuelven en unos pocos días a unas pocas semanas.
Los informes de dolor en el lugar de la inyección fueron más frecuentes con Lantus que con la insulina humana NPH (2,7% de insulina glargina versus 0,7% de NPH). Los informes de dolor en el sitio de inyección fueron generalmente leves y no dieron lugar a la interrupción de la terapia.
Las reacciones alérgicas de tipo inmediato son raras. Tales reacciones a la insulina (incluida la insulina glargina) o los excipientes pueden, por ejemplo, estar asociadas con reacciones cutáneas generalizadas, angioedema, broncoespasmo, hipotensión o shock y puede ser de por vida amenazante.
Condiciones intercurrentes
Los requisitos de insulina pueden alterarse durante condiciones intercurrentes como enfermedades, trastornos emocionales o estrés.
Información para pacientes
Lantus solo debe usarse si la solución es transparente e incolora sin partículas visibles (ver DOSIFICACIÓN Y ADMINISTRACIÓN, Preparación y manejo).
Se debe informar a los pacientes que Lantus NO se debe diluir ni mezclar con ninguna otra insulina o solución (ver PRECAUCIONES, General).
Se debe instruir a los pacientes sobre los procedimientos de autogestión, incluida la monitorización de la glucosa, la técnica de inyección adecuada y el manejo de la hipoglucemia y la hiperglucemia. Se debe instruir a los pacientes sobre el manejo de situaciones especiales como condiciones intercurrentes (enfermedad, estrés o trastornos emocionales). trastornos), una dosis de insulina inadecuada u omitida, administración inadvertida de una dosis aumentada de insulina, ingesta inadecuada de alimentos o comidas omitidas Remita a los pacientes a la circular "Información del paciente" de Lantus para obtener información adicional.
Al igual que con todos los pacientes con diabetes, la capacidad de concentración y / o reacción puede verse afectada como resultado de la hipoglucemia o la hiperglucemia.
Se debe aconsejar a las pacientes con diabetes que informen a su profesional de la salud si están embarazadas o si están contemplando un embarazo.
Interacciones con la drogas
Varias sustancias afectan el metabolismo de la glucosa y pueden requerir un ajuste de la dosis de insulina y, en particular, una estrecha vigilancia.
Los siguientes son ejemplos de sustancias que pueden aumentar el efecto reductor de la glucosa en sangre y la susceptibilidad a la hipoglucemia: productos antidiabéticos orales, Inhibidores de la ECA, disopiramida, fibratos, fluoxetina, inhibidores de la MAO, propoxifeno, salicilatos, análogo de somatostatina (por ejemplo, octreotida), sulfonamida antibióticos
Los siguientes son ejemplos de sustancias que pueden reducir el efecto hipoglucemiante de la insulina: corticosteroides, danazol, diuréticos, agentes simpaticomiméticos (p. ej., epinefrina, albuterol, terbutalina), isoniacida, derivados de fenotiazina, somatropina, hormonas tiroideas, estrógenos, progestágenos (por ejemplo, en anticonceptivos orales), inhibidores de la proteasa y medicamentos antipsicóticos atípicos (por ejemplo, olanzapina y clozapina).
Los betabloqueantes, la clonidina, las sales de litio y el alcohol pueden potenciar o debilitar el efecto hipoglucemiante de la insulina. La pentamidina puede causar hipoglucemia, que a veces puede ser seguida de hiperglucemia.
Además, bajo la influencia de medicamentos simpaticolíticos como los betabloqueantes, la clonidina, la guanetidina y la reserpina, los signos de hipoglucemia pueden estar reducidos o ausentes.
Carcinogénesis, Mutagénesis, Deterioro de la Fertilidad
En ratones y ratas, se realizaron estudios de carcinogenicidad estándar de dos años con insulina glargina a dosis de hasta 0.455 mg / kg, que es para la rata aproximadamente 10 veces y para el ratón aproximadamente 5 veces la dosis inicial subcutánea humana recomendada de 10 UI (0,008 mg / kg / día), basada en mg / m2. Los hallazgos en ratones hembra no fueron concluyentes debido a la mortalidad excesiva en todos los grupos de dosis durante el estudio. Se encontraron histiocitomas en los sitios de inyección en ratas macho (estadísticamente significativas) y ratones machos (no estadísticamente significativos) en grupos que contienen vehículos ácidos. Estos tumores no se encontraron en animales hembras, en el control de solución salina o en grupos de comparación de insulina usando un vehículo diferente. Se desconoce la relevancia de estos hallazgos para los humanos.
La insulina glargina no fue mutagénica en las pruebas para la detección de mutaciones genéticas en bacterias y células de mamíferos (Ames y Prueba HGPRT) y en pruebas para la detección de aberraciones cromosómicas (citogenética in vitro en células V79 e in vivo en chino hamsters)
En un estudio combinado de fertilidad y prenatal y posnatal en ratas machos y hembras a dosis subcutáneas de hasta 0,36 mg / kg / día, que es aproximadamente 7 veces el Se recomendó la dosis inicial subcutánea humana de 10 UI (0,008 mg / kg / día), basada en mg / m2, la toxicidad materna debida a la hipoglucemia dependiente de la dosis, incluidas algunas muertes. observado. En consecuencia, se produjo una reducción de la tasa de cría en el grupo de dosis alta solamente. Se observaron efectos similares con la insulina humana NPH.
El embarazo
Efectos teratogénicos
Embarazo Categoría C. Se han realizado estudios de reproducción subcutánea y teratología con insulina glargina e insulina humana regular en ratas y conejos del Himalaya. El medicamento se administró a ratas hembras antes del apareamiento, durante el apareamiento y durante todo el embarazo a dosis de hasta 0,36 mg / kg / día. que es aproximadamente 7 veces la dosis inicial subcutánea humana recomendada de 10 UI (0,008 mg / kg / día), según mg / m2. En conejos, dosis de 0.072 mg / kg / día, que es aproximadamente 2 veces la recomendada para humanos Se administraron dosis iniciales subcutáneas de 10 UI (0,008 mg / kg / día), basadas en mg / m2, durante organogénesis Los efectos de la insulina glargina generalmente no diferían de los observados con insulina humana regular en ratas o conejos. Sin embargo, en conejos, cinco fetos de dos camadas del grupo de dosis alta mostraron dilatación de los ventrículos cerebrales. La fertilidad y el desarrollo embrionario temprano parecían normales.
No existen estudios clínicos bien controlados sobre el uso de insulina glargina en mujeres embarazadas. Es esencial que los pacientes con diabetes o antecedentes de diabetes gestacional mantengan un buen control metabólico antes de la concepción y durante todo el embarazo. Los requerimientos de insulina pueden disminuir durante el primer trimestre, generalmente aumentar durante el segundo y tercer trimestre y disminuir rápidamente después del parto. El monitoreo cuidadoso del control de glucosa es esencial en tales pacientes. Debido a que los estudios de reproducción en animales no siempre predicen la respuesta humana, este medicamento debe usarse durante el embarazo solo si es claramente necesario.
Madres lactantes
Se desconoce si la insulina glargina se excreta en cantidades significativas en la leche humana. Muchas drogas, incluida la insulina humana, se excretan en la leche humana. Por esta razón, se debe tener precaución cuando Lantus se administra a una mujer lactante. Las mujeres lactantes pueden requerir ajustes en la dosis de insulina y la dieta.
Uso pediátrico
La seguridad y eficacia de Lantus se han establecido en el grupo de edad de 6 a 15 años con diabetes tipo 1.
Uso geriátrico
En estudios clínicos controlados que compararon insulina glargina con insulina humana NPH, 593 de 3890 pacientes con diabetes tipo 1 y tipo 2 tenían 65 años o más. La única diferencia en seguridad o efectividad en esta subpoblación en comparación con toda la población de estudio fue una mayor incidencia esperada de eventos cardiovasculares tanto en insulina glargina como en NPH humana tratada con insulina pacientes
En pacientes de edad avanzada con diabetes, la dosis inicial, los incrementos de dosis y la dosis de mantenimiento deben ser conservadores para evitar reacciones hipoglucémicas. La hipoglucemia puede ser difícil de reconocer en los ancianos (ver PRECAUCIONES, Hipoglucemia).
parte superior
Reacciones adversas
Los eventos adversos comúnmente asociados con Lantus incluyen los siguientes:
Cuerpo en su conjunto: reacciones alérgicas (ver PRECAUCIONES).
Piel y apéndices: reacción en el lugar de inyección, lipodistrofia, prurito, erupción cutánea (ver PRECAUCIONES).
Otro: hipoglucemia (ver Advertencias y PRECAUCIONES).
En estudios clínicos en pacientes adultos, hubo una mayor incidencia de dolor en el lugar de inyección emergente del tratamiento en pacientes tratados con Lantus (2.7%) en comparación con pacientes tratados con insulina NPH (0.7%). Los informes de dolor en el sitio de inyección fueron generalmente leves y no dieron lugar a la interrupción de la terapia. Se produjeron otras reacciones en el lugar de inyección emergentes del tratamiento con incidencias similares tanto con insulina glargina como con insulina humana NPH.
La retinopatía se evaluó en los estudios clínicos mediante eventos adversos de la retina informados y fotografía de fondo de ojo. El número de eventos adversos retinianos informados para los grupos de tratamiento de Lantus y NPH fue similar para los pacientes con diabetes tipo 1 y tipo 2. La progresión de la retinopatía se investigó mediante fotografía de fondo de ojo utilizando un protocolo de clasificación derivado del Estudio de retinopatía diabética de tratamiento temprano (ETDRS). En un estudio clínico con pacientes con diabetes tipo 2, una diferencia en el número de sujetos con â ‰ ¥ 3 pasos la fotografía de fondo de ojo observó una progresión en la escala ETDRS durante un período de 6 meses (7.5% en el grupo Lantus versus 2.7% en NPH grupo tratado). La relevancia general de este hallazgo aislado no se puede determinar debido al pequeño número de pacientes involucrado, el corto período de seguimiento y el hecho de que este hallazgo no se observó en otras clínicas estudios.
parte superior
Sobredosis
Un exceso de insulina en relación con la ingesta de alimentos, el gasto de energía, o ambos, puede conducir a una hipoglucemia grave, a veces a largo plazo y potencialmente mortal. Los episodios leves de hipoglucemia generalmente se pueden tratar con carbohidratos orales. Es posible que se necesiten ajustes en la dosis del medicamento, los patrones de comida o el ejercicio.
Los episodios más graves con coma, convulsiones o deterioro neurológico pueden tratarse con glucagón intramuscular / subcutáneo o glucosa intravenosa concentrada. Después de la aparente recuperación clínica de la hipoglucemia, puede ser necesaria la observación continuada y la ingesta adicional de carbohidratos para evitar la recurrencia de la hipoglucemia.
parte superior
Dosificación y administración
Lantus es un análogo de insulina humana recombinante. Su potencia es aproximadamente la misma que la insulina humana. Presenta un perfil de reducción de glucosa relativamente constante durante 24 horas que permite la dosificación una vez al día.
Lantus puede administrarse en cualquier momento durante el día. Lantus debe administrarse por vía subcutánea una vez al día a la misma hora todos los días. Para pacientes que ajustan el tiempo de dosificación con Lantus, ver Advertencias y PRECAUCIONES, Hipoglucemia Lantus no está destinado a la administración intravenosa (ver PRECAUCIONES). La administración intravenosa de la dosis subcutánea habitual puede provocar hipoglucemia grave. Los niveles de glucosa en sangre deseados, así como las dosis y el momento de los medicamentos antidiabéticos, deben determinarse individualmente. La monitorización de la glucosa en sangre se recomienda para todos los pacientes con diabetes. La duración prolongada de la actividad de Lantus depende de la inyección en el espacio subcutáneo.
Al igual que con todas las insulinas, los sitios de inyección dentro del área de inyección (abdomen, muslo o deltoides) deben rotarse de una inyección a la siguiente.
En estudios clínicos, no hubo diferencias relevantes en la absorción de insulina glargina después de la administración subcutánea abdominal, deltoidea o del muslo. Como para todas las insulinas, la tasa de absorción y, en consecuencia, el inicio y la duración de la acción, pueden verse afectados por el ejercicio y otras variables.
Lantus no es la insulina de elección para el tratamiento de la cetoacidosis diabética. La insulina intravenosa de acción corta es el tratamiento preferido.
Uso pediátrico
Lantus se puede administrar de forma segura a pacientes pediátricos de ¥ 6 años de edad. Administración a pacientes pediátricos.
Iniciación de la terapia Lantus
En un estudio clínico con pacientes ingenuos de insulina con diabetes tipo 2 ya tratados con medicamentos antidiabéticos orales, Lantus se inició en una dosis promedio de 10 UI una vez al día, y posteriormente ajustada según la necesidad del paciente a una dosis diaria total que varía de 2 a 100 IU
Cambio a Lantus
Si cambia de un régimen de tratamiento con una insulina de acción intermedia o prolongada a un régimen con Lantus, la cantidad y el momento de la insulina de acción corta o el análogo de insulina de acción rápida o la dosis de cualquier medicamento antidiabético oral puede necesitar ser equilibrado. En estudios clínicos, cuando los pacientes fueron transferidos de insulina humana NPH una vez al día o insulina humana ultralente a Lantus una vez al día, la dosis inicial generalmente no cambió. Sin embargo, cuando los pacientes fueron transferidos de insulina humana NPH dos veces al día a Lantus una vez al día, para reducir el riesgo de hipoglucemia, la la dosis (UI) generalmente se redujo en aproximadamente un 20% (en comparación con la UI diaria total de insulina humana NPH) y luego se ajustó en función de la respuesta del paciente (ver PRECAUCIONES, Hipoglucemia).
Se recomienda un programa de monitoreo metabólico cercano bajo supervisión médica durante la transferencia y en las semanas iniciales posteriores. Es posible que sea necesario ajustar la cantidad y el momento de la insulina de acción corta o el análogo de insulina de acción rápida. Esto es particularmente cierto para pacientes con anticuerpos adquiridos contra la insulina humana que necesitan dosis altas de insulina y ocurre con todos los análogos de insulina. Puede ser necesario ajustar la dosis de Lantus y otras insulinas o medicamentos antidiabéticos orales; por ejemplo, si el momento de dosificación, el peso o el estilo de vida del paciente cambian u otras circunstancias que aumentan la susceptibilidad a la hipoglucemia o hiperglucemia (ver PRECAUCIONES, Hipoglucemia).
La dosis también puede tener que ajustarse durante una enfermedad intercurrente (ver PRECAUCIONES, Condiciones intercurrentes).
Preparación y manejo
Los productos farmacológicos parenterales deben inspeccionarse visualmente antes de la administración siempre que la solución y el envase lo permitan. Lantus solo debe usarse si la solución es transparente e incolora sin partículas visibles.
Mezcla y dilución: Lantus NO debe diluirse ni mezclarse con ninguna otra insulina o solución (ver PRECAUCIONES, General).
Vial: las jeringas no deben contener ningún otro medicamento o residuo.
Sistema de cartucho: si OptiClik®, el dispositivo de administración de insulina para Lantus, funciona mal, Lantus puede extraerse del sistema de cartucho en una jeringa U-100 e inyectarse.
parte superior
Cómo se suministra
Lantus 100 unidades por ml (U-100) está disponible en el siguiente tamaño de paquete:
Viales de 10 ml (NDC 0088-2220-33)
Sistema de cartucho de 3 ml1, paquete de 5 (NDC 0088-2220-52)
1Los sistemas de cartucho son para uso exclusivo en OptiClik® (dispositivo de administración de insulina)
Almacenamiento
Vial sin abrir / sistema de cartucho
Los viales de Lantus sin abrir y los sistemas de cartucho deben almacenarse en un refrigerador, 36 ° F - 46 ° F (2 ° C - 8 ° C). Lantus no debe almacenarse en el congelador y no debe permitirse que se congele.
Desechar si se ha congelado.
Sistema de vial / cartucho abierto (en uso)
Los viales abiertos, refrigerados o no, deben usarse dentro de los 28 días posteriores al primer uso. Deben descartarse si no se usan dentro de los 28 días. Si no es posible la refrigeración, el vial abierto se puede mantener sin refrigerar hasta 28 días lejos del calor y la luz directa, siempre que la temperatura no sea superior a 86 ° F (30 ° C).
El sistema de cartucho abierto (en uso) en OptiClik® NO debe refrigerarse, sino que debe mantenerse a temperatura ambiente (por debajo de 86 ° F [30 ° C]) lejos del calor directo y la luz. El sistema de cartucho abierto (en uso) en OptiClik® mantenido a temperatura ambiente debe desecharse después de 28 días. No almacene OptiClik®, con o sin sistema de cartucho, en un refrigerador en ningún momento.
Lantus no debe almacenarse en el congelador y no debe permitirse que se congele. Desechar si se ha congelado.
Estas condiciones de almacenamiento se resumen en la siguiente tabla:
| No esta en uso (sin abrir) Refrigerado |
No esta en uso (sin abrir) Temperatura ambiente |
En uso (abrió) (Ver temperatura abajo) |
|
|---|---|---|---|
| 10 ml de vial | Hasta la fecha de vencimiento | 28 dias | 28 dias Refrigerado o a temperatura ambiente |
| Sistema de cartucho de 3 ml | Hasta la fecha de vencimiento | 28 dias | 28 dias Refrigerado o a temperatura ambiente |
| Cartucho de 3 ml sistema insertado en OptiClik® |
28 dias Temperatura ambiente solamente (No refrigerar) |
Fabricado para un distribuido por:
sanofi-aventis U.S. LLC
Bridgewater NJ 08807
Hecho en Alemania
www. Lantus.com
© 2006 sanofi-aventis U.S. LLC
OptiClik® es una marca registrada de sanofi-aventis U.S. LLC, Bridgewater NJ 08807
última actualización 04/2006
Lantus, insulina glargina (origen de ADNr), información del paciente (en inglés simple)
Información detallada sobre signos, síntomas, causas, tratamientos de diabetes
La información de esta monografía no pretende abarcar todos los usos, instrucciones, precauciones, interacciones farmacológicas o efectos adversos posibles. Esta información es generalizada y no pretende ser un consejo médico específico. Si tiene preguntas sobre los medicamentos que está tomando o desea obtener más información, consulte con su médico, farmacéutico o enfermero.
de regreso: Ver todos los medicamentos para la diabetes



